先生が研究されている「生理活性物質」とはどんな物質ですか?
生命活動を維持・調節するために必要な化学物質の総称です。生物間の相互作用にも大きな役割を果たしており、例えば、植物と昆虫との間でも生理活性物質が働いています。昆虫が植物を食べようとするとき、植物はただ食べられるのではなく、忌避効果のある物質を生成したり、周囲の環境に働きかけたりして昆虫を寄せ付けないように防除します。このとき植物が出す物質をうまく使えば、自然に優しい農薬ができるかもしれません。
私の研究は有用な生理活性物質を探索するとともに、それらが機能するメカニズムを解明することです。生理活性物質はタンパク質と結合することで、生体内のさまざまな生理作用を引き起こします。研究ではタンパク質の“形”を切り口に、タンパク質と生理活性物質との相互作用の関係を調べています。タンパク質の形がわかると、それに基づいて確度の高いシミュレーションが可能になります。

タンパク質の形というのは...?
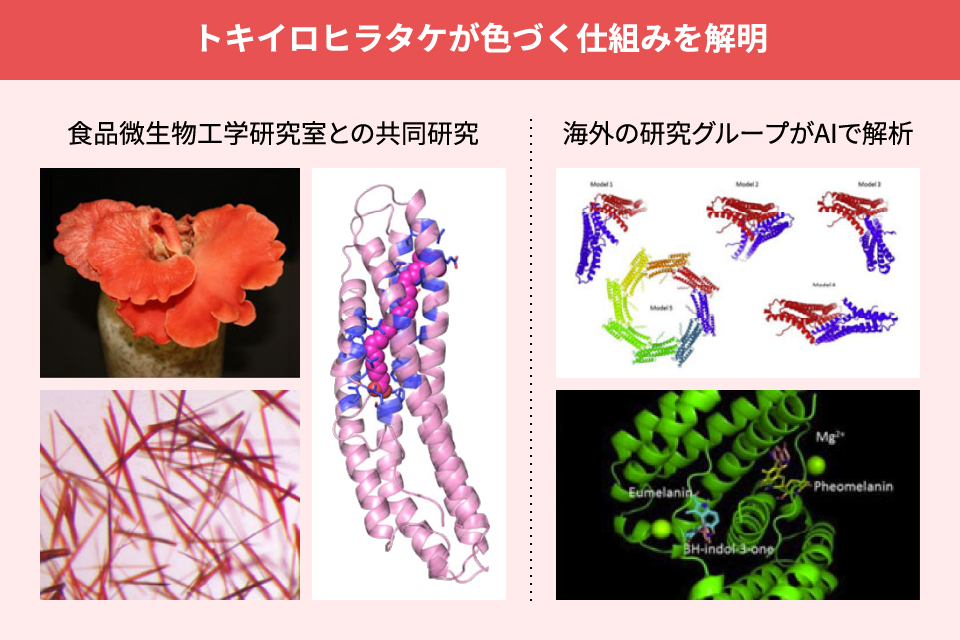
一例ですが、下の絵がタンパク質の形です。これはトキイロヒラタケという食用キノコで、鳥のトキのような色をしています。トキイロヒラタケの色素タンパク質を結晶化して、X線結晶構造解析というテクニックで分析すると、こんな形をしているのがわかりました。この研究で私たちのグループは、トキイロヒラタケの発色メカニズムを明らかにしています。中央にある団子状のものが色の原因物質です。そして右側の図。これはごく最近、海外の研究グループがトキイロヒラタケの色の付く仕組みをAIで解明したという報告です。両者はまったく違う形をしていることがわかりますが、AIによる間違った解析が学術論文で発表されているのです。このとき使われたAIはタンパク質の構造予測を実行する先端の人工知能プログラムで、それでもまったく違った形が導き出されていました。AIはこれまでに何らかの形で発表されたデータを元に学習し動いていますので、未知のものに対しては間違った結果を与えることがあります。最近はAIの進化が目覚ましいといわれますが、実験データに基づいた地道な研究はやはり大切ということですね。
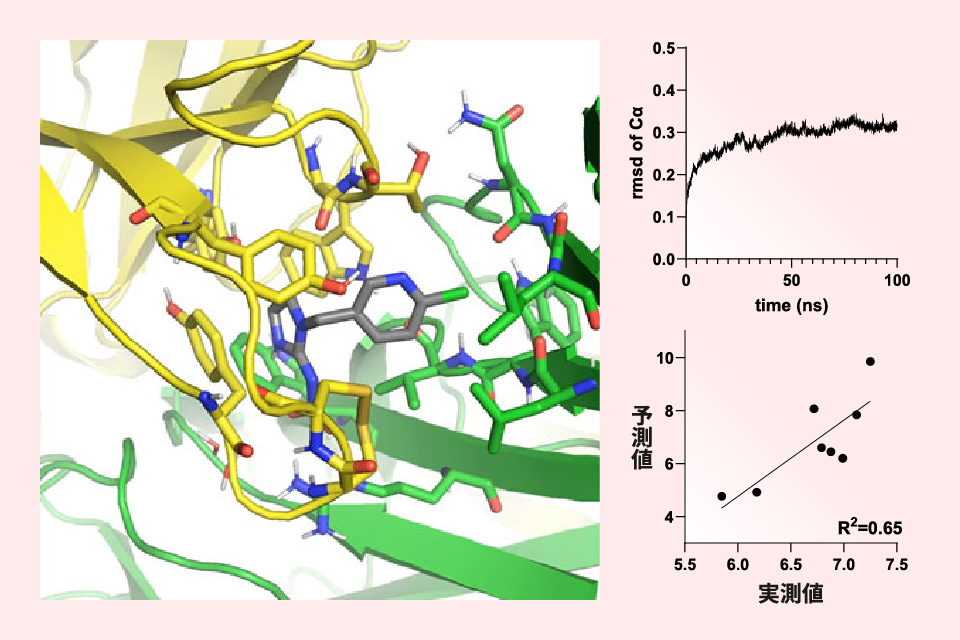
技術系の開発研究も行っており、薬品の効き具合をシミュレーションする技術の開発に取り組んできました。下の図はタンパク質と農薬が結合した状態をシミュレーションしたもので、農薬の候補になる薬がタンパク質とどのくらい強く結合するのかを予測しています。この形は計算で出した予測の構造です。薬を生体内に取り込むと、作用点であるタンパク質までたどり着いて結合します。図はその際の相互作用のようすを示しています。右横にグラフがありますが、「実測値」という横軸が実験で確かめた強さで、縦軸が「予測値」。実測値と予測値が比例関係にあるという結果が得られています。これは大事なことで、実測には時間がかかるうえに、人手も必要で、それなりに薬品も使います。この予測値はコンピュータに計算を指示してやれば、自動的に算出されます。薬の構造をデザインして、その予測値が高い数値を示せば実測値も高くなると推定でき、強い薬になる可能性があるということを実験することなく予想できます。
薬の標的というのは1カ所ではありません。同じ薬でもさまざまなタンパク質に結合しますので、その種々のタンパク質をコンピュータの中で準備して、どれに効いて、どれに効かないといった情報も蓄積できます。薬の効き目はずっと同じではなく、標的が薬剤に対して耐性を持ってしまう問題が起こります。この情報が数多くストックできれば、薬剤耐性という問題についても予測できるようになります。

すごくおもしろいですね、この動画は薬剤とタンパク質が結合したときの状態ですか?
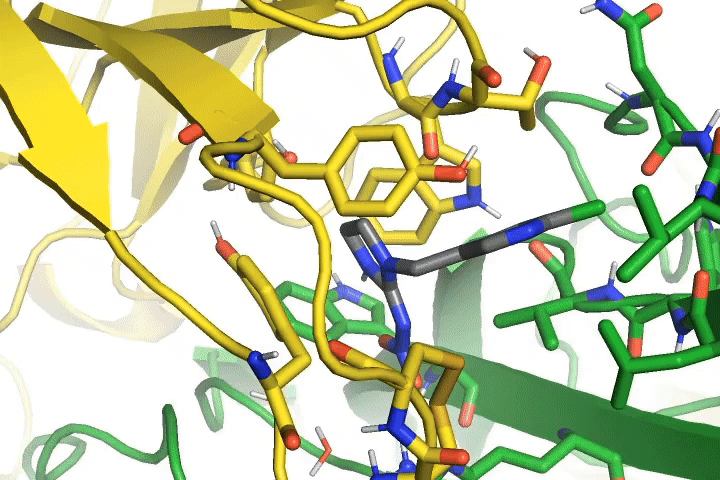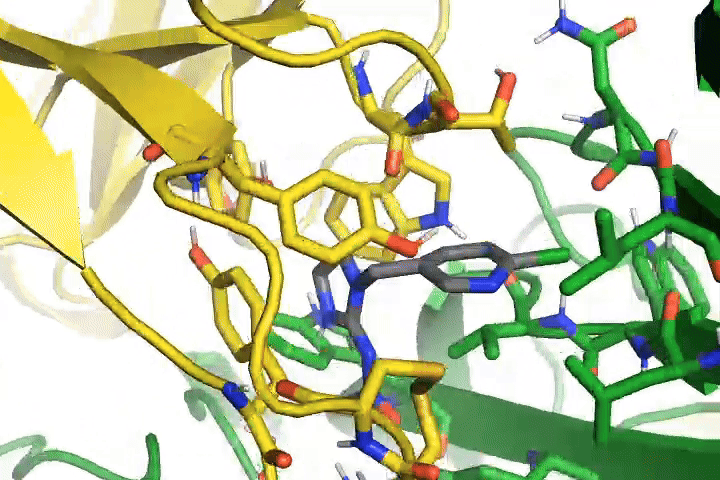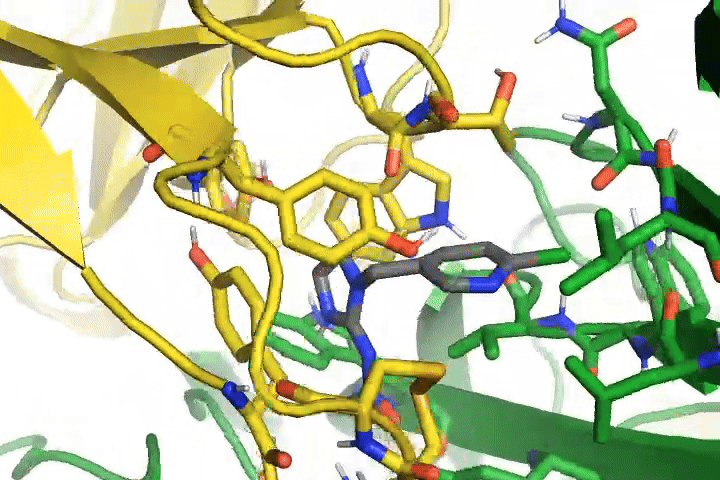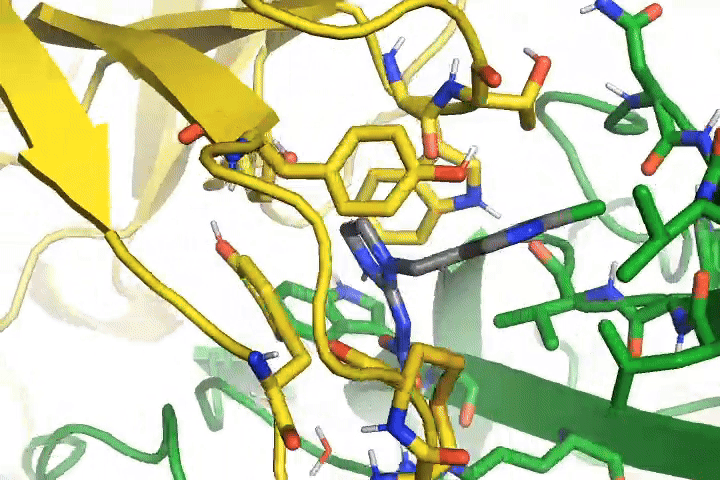
はい。この動画は虫の神経上にあるタンパク質に、薬が結合している状態です。黄色と緑がタンパク質で、グレーが薬。タンパク質の間に薬が挟まっているようすがわかります。この薬はタンパク質に結合すると虫の神経を異常興奮させ、その働きを妨害して動けなくするという機能を持っています。ちなみに、動いているのは熱振動による揺らぎで、原子・分子は絶えず振動しています。実際の振動はこの動画とは比較にならないほど速いスピードです。
タンパク質には膨大な種類があり、すべての形はわかっているわけではありません。わかっているのはヒトの受容体などほんの一部。昆虫の受容体はわかっていませんので、この形は予想です。コンピュータの中で形を予測したうえで受容体をつくり、薬を反応させて相互作用の強さを測っています。実測では研究室で動物の細胞を使って受容体を作成し、それに対して薬を掛けて薬の効き具合を評価します。予想の構造に基づいて薬の効き具合をシミュレーションした結果と、実際に測定した値が合致すれば、かなり確度の高い予測だといえるでしょう。
実験における測定の手法としては、電気生理という方法を用います。細胞の活動を電気的に測る実験方法で、身近なところでいえば心電図や脳波測定も電気生理の一種です。薬をかけるとタンパク質が働き、そのタンパク質が電気を通すようになります。そのときに細胞の表面を流れる電流を測って神経の働きを調べます。この「昆虫の単一神経細胞の活動を電流として記録する技術」はかなり以前のことですが、私自身がつくったものです。それ以前は1分程度の短時間でしかできなかったのですが、より長時間にわたって測定できるように技術開発したことで、さまざまな薬を掛けて効き具合を試せるようになりました。

先生の研究はどんな分野に生かされますか?
大きくいえば農薬、殺虫剤の成分です。新しい農薬になるかもしれない物質候補を見いだすだけでなく、すでに知られている農薬についても、メカニズムを研究していきたいと考えています。というのは、農薬は効果と安全性が立証できれば製品化が可能であり、効くメカニズムまでわかっていない薬剤も存在します。もちろん、現在販売されている農薬は十分な安全性を備えていますが、原子・分子レベルでそのしくみを明らかにすれば、それらをより良くできます。今のメジャーな農薬は、防虫効果があり人には効かないというのは良いのですが、一方でミツバチなどの益虫にまで効いてしまうという問題点があります。それを特定の虫にだけ効くようにできるかもしれません。企業は農薬の開発にあたって、活性の強い物質を見つけているので、それは研究のツールになります。効くかどうかわからない物質で研究をスタートさせるとなかなか答えが出ません。確実に効く物質を相手に研究すると、早く答えにたどり着ける可能性が高まります。
これからも生理活性物質の作用機構を解き明かすことをテーマに、サイエンスを深めていきたいと考えています。






